İlgili Yazı
XL-MS ile Membran Proteinlerini Analiz Edin: Adım Adım İş Akışı Rehberi
2026-02-20XL-MS ile Membran Proteinlerini Analiz Etmek, "görülmesi zor" membran etkileşimlerini ölçülebilir kanıta dönüştürmenin en pratik yollarından biridir. Longlight Teknolojisi, araştırmacıların protein-protein etkileşimlerini (PPI'ler) haritalamasına, zayıf veya kısa ömürlü temasları yakalamasına ve hipotezlerden savunulabilir yapısal modellere geçişine yardımcı olmak için kimyasal çapraz bağlama ve kütle spektrometrisi (XL-MS) ile birleştirilerek özel kimyasal etiketleme iş akışlarını zorlamadan yardımcı olur.
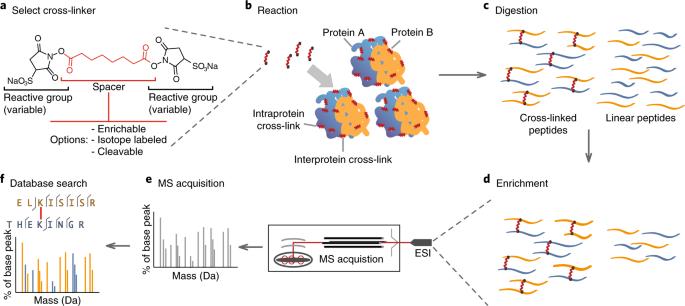
Çapraz bağlamalı kütle spektrometrisi: yapısal, moleküler ve sistemlerde yöntemler ve uygulamalar
XL-MS nedir? Zar Proteinleri Nedir?
XL-MS ve zar proteinleri, yapısal biyoloji ve ilaç keşfinde sıkça birlikte görülen iki fikirdir. İşte açık, yeni başlayanlar için uygun bir açıklama.
XL-MS nedir?
XL-MS (İngilizce) çapraz bağlama kütle spektrometrisi anlamına gelir (genellikle kimyasal çapraz bağlama ve kütle spektrometrisi olarak yazılır).
Protein-protein etkileşimlerini ve protein şekillerini incelemek için iki yöntemle kullanılır:
Çapraz bağlama (XL): Yakındaki parçaları yerinde "dondur"
Kimyasal çapraz bağlayıcı, küçük bir moleküler "köprü" gibi davranır. Eğer iki amino-asit sitesi gerçek uzayda (kısa mesafede) yeterince yakınsa, çapraz bağlayıcı onları kovalent olarak bağlayabilir.
Bu, normal örnek işlenmesi sırasında bozulmaya yol açabilecek zayıf veya kısa süreli etkileşimleri korumaya yardımcı olur.
Kütle Spektrometrisi (MS): Bağlantılı parçaları belirleyin
Çapraz bağlamadan sonra proteinler peptitlere dönüştürülür. Kütle spektrometresi, çapraz bağlı peptit çiftlerini tespit eder ve yazılım bunları proteinlere geri eşler.
Bu bağlantılar, orijinal komplekste hangi bölgelerin yakın olduğunu söyleyen mesafe ipuçları (mekansal kısıtlamalar) sağlar.
XL-MS size (pratikte) ne söylüyor:
• Hangi proteinlerin muhtemelen etkileşime girdiği (etkileşim ağı)
• Hangi bölgeler temas ediyor (arayüz ipuçları)
• Modelleri destekleyen yapısal kısıtlamalar (genellikle kriyo-EM veya X-ışını ile birleşir)
Zar Proteinleri Nedir?
Zar proteinleri, hücre zarına (veya hücrelerin içindeki membranlara, örneğin ER, mitokondri veya bakteri zarları) gömülü veya ona bağlı olan proteinlerdir.
Bunlar kritik çünkü zarlar taşınmayı ve sinyal iletimi kontrol eder ve zar proteinleri genellikle hücre için "kapı bekçisi" veya "anten" olarak görev yapar.
Ana Tipler
• Integral zar proteinleri: zarın içinde fiziksel olarak gömülü
• Birçoğu zarı bir veya birden fazla kez kaplar (genellikle transmembran proteinler olarak adlandırılır)
• Çevresel zar proteinleri: membran yüzeyine (genellikle diğer proteinler veya lipidler aracılığıyla) bağlıdır
Neden Zar Proteinleri Önemlidir
• Aşağıdaki alanlarda yer alırlar:
• Taşıma (kanallar, pompalar, taşıyıcılar)
• Hücre sinyalizasyonu (GPCR gibi reseptörler)
• Enerji dönüşümü (solunum zinciri kompleksleri)
• Hücre tanıma ve yapışma
Neden "Zor" Oldukları
Zar proteinlerinin incelenmesi zordur çünkü:
• Lipid ortamında otururlar
• Zardan çıkarıldıklarında kararsız olabilirler
• Genellikle durumları değiştiren dinamik kompleksler oluştururlar
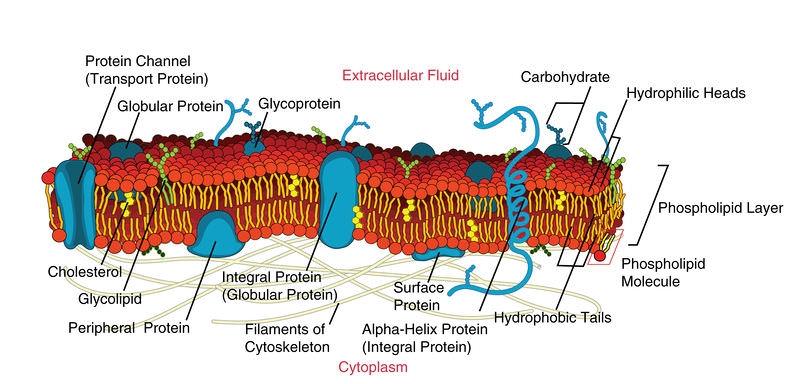
Zar Proteinleri - Biyoloji LibreMetinleri
Neden Zar Proteinleri Gereklidir a Farklı Stratejiler
Zar proteinleri genellikle kalabalık, dinamik ortamlarda bulunur. Ana arayüzleri geçici olabilir ve birçok kompleks zardan çıkarıldıktan sonra kararsız hale gelir. Bu yüzden klasik etkileşim yöntemleri kritik temasları kaçırabilir veya olup bitenleri aşırı basitleştirebilir.
XL-MS ile Membran Proteinlerini Analiz Etmek, yakın bölgeleri çapraz bağlama ajanları kullanarak yerinde "dondurması" sayesinde işe yarar. Bu reaktifler, belirli bir mesafe penceresi içinde iki veya daha fazla etkileşimli proteini kovalent olarak bağlayabilir. Etkileşim kilitlendikten sonra, kütle spektrometrisi çapraz bağlı peptitleri okuyabilir ve sizi muhtemel temas noktalarına yönlendirebilir. Operasyonel olarak, etkileşim kanıtları kompleksler zayıf olsa bile izlenebilir kalır.
• Temizlenme sırasında sıklıkla kaybedilen kısa süreli etkileşimleri güvence altına alır
• Kimyasal etiketlemeden kaçınır, erken kararları kolaylaştırır
• Yerel yakınlığı korumak için hücre içi çapraz bağlama imkanı sağlar
Adım 1: Biyolojik soruyu ve mesafe gerekçesini belirtin
Başlamadan önce ne öğrenmek istediğinize karar verin. Şüpheli bir ortağı doğruluyor musunuz? Mutant ile wild tipi bağlamayı karşılaştırmak mı? Bir arayüzü bir modeli desteklemek için eşleme mi yapılıyor? Net bir soru, koşulları, kontrolleri ve veri çıktılarını seçmenize yardımcı olur.
XL-MS mesafe bilgilidir. Çapraz bağlama ajanları, mekânda yakın olan kalıntıları bağlar, mutlaka bitişik sırada değiller. Zar proteinleri için bu mesafe mantığı değerlidir çünkü helikslerin nasıl paketlendiğini, sitozolik döngülerin temas partnerleriyle nasıl birleştiğini veya oligomerlerin nasıl birleştiğini ortaya koyabiliyor.
Planınızı yeni başlayanlar için uygun bir şekilde çerçevelemek için üç çıkış tanımlamaktır:
• Etkileşim Varlığı: A B ile hiç iletişim kuruyor mu?
• Etkileşim Topolojisi: A'nın hangi bölgeleri B'nin hangi bölgeleriyle temas eder?
• Site Kanıtı: Hangi peptid çiftleri etkileşim ağını destekler?
XL-MS ile Membran Proteinlerini Analiz Etmek, bir sonraki kararınızda hangilerine ihtiyacınız olduğunu önceden belirlediğinizde (yapı modelleme, hedef doğrulama veya mekanizma çalışması) çok daha akıcı hale gelir.
Adım 2: Seç a Membran Bağlamına Uygun Çapraz Bağlama Yaklaşımı
Zar proteinleri deterjanlara, lipid mimetiklerine ve tampon bileşimine karşı hassastır. Amaç, fonksiyonel komplekse mümkün olduğunca yakın bir durumu korumak ve ardından doğru anda çapraz bağlantı kurmaktır.
Longlight Technology'de müşteriler önceden çapraz bağlanmış örnekleri gönderebilir veya çapraz bağlama planı geliştirmek için bizimle iletişime geçip numune gönderebilirler. Bu esneklik, membran hedefleri için önemlidir çünkü bir proje çözüm içi çapraz bağlama gerektirebilirken, diğeri daha doğal koşullar veya hatta hücre içi çapraz bağlama ile fayda sağlar.
✔ Yüksek veri verimliliği ve hızlı analiz hızı, yineleme döngülerini kısaltabilir
✔ Hücre içi çapraz bağlama, aşırı işleme komplekslerinden kaynaklanan artefaktları azaltabilir
✔ Özel bir etiketleme gereksinimi olmadan erken deneylerin erişilebilir olmasını sağlar
Yeni başlayanlar için pratik ipucu: en az bir negatif kontrol planı yapın (çapraz bağlayıcı veya partner proteini yok) ve varsa bir "bilinen davranış" referansı yapın. Kontroller, gerçek yakınlık sinyallerini arka plandan ayırt etmenize yardımcı olur.
Adım 3: Çapraz Bağlı Proteinlerden to Tespit edilebilir Peptitler
Çapraz bağlamadan sonra, iş akışı proteinleri çapraz bağlantı bilgisini koruyan bir peptit karışımına çevirmelidir. Birçok yeni başlayan kişi burada kendini kaybolmuş hisseder, çünkü çapraz bağlı peptidler normal peptitlerden daha nadirdir ve tespit edilmesi daha zor olabilir.
Standart hizmet iş akışımız tüm zinciri kapsar:
• Enzim sindirimi
• Peptit zenginleştirme
• Kütle spektrometrisi tespiti
• Veri analizi
• Deneysel rapor teslimatı
Ana fikir basittir: sindirim proteinleri peptitlere dönüştürür, zenginleştirme çapraz bağlı türlerin göreceli görünürlüğünü artırır ve kütle spektrometrisi peptit kütlelerini ve parçalarını ölçür böylece yazılım çapraz bağlantı çiftlerini atayarabiler.
XL-MS ile Membran Proteinlerini Analiz Etmek, örnek hazırlığını sadece rutin bir protokol değil, bilgi koruma adımı olarak ele aldığınızda en verimli olur. En iyi sonuçlar, kararlı sindirim ve dikkatli zenginleştirmeden gelir; böylece veriler güvenilir yorum için yeterli sinyal taşır.
Adım 4: Kütle Spektrometrisi Okuması and Etkileşim Ağı Haritalaması
Kütle spektrometrisi sadece "proteinleri tanımlamak" yapmıyor. XL-MS'de, çapraz bağlı peptid çiftlerini tanımlar; bunları mekânsal kısıtlamalar olarak yorumlayabilirsiniz. Yeterince yüksek güvenli bağlantıya sahip olduğunuzda, etkileşim ağlarını tasvir etmeye ve eylem noktalarını çıkarmaya başlayabilirsiniz—özellikle karmaşık zar montajları için faydalıdır.
Burada XL-MS aynı zamanda yapısal biyolojiye bir köprü haline gelir. Birçok ekip XL-MS çıkışlarını kriyo-EM veya X-ışını kristalografisiyle birlikte kullanır. Çapraz bağlantı kanıtları yardımcı olabilir:
• Yapısal bir modelin makul olup olmadığını doğrulamak
• Belirsiz alt birim yönelimlerini çöz
• Yoğunluk sınırlı olduğunda alan yerleşimini destekle
Başka bir deyişle, XL-MS ile Membran Proteinlerini Analiz Etmek sizi "bu iki bölgenin etkileştiğini düşünüyoruz" durumundan, "modeli kısıtlayan mesafe destekli kanıtlarımıza sahibiz" kavramına taşıyabilir.
Adım 5: Nasıl to Oku tRapor aVeriyi Sonraki Deneylere Dönüştürün
Bir rapor ancak kararları yönlendiriyorsa değerlidir. Yeni başlayanlar için XL-MS sonuçlarını okumanın en faydalı yolu sadece listelere değil, desenlere bakmaktır.
Üç soruyla başlayın:
✔ Çapraz bağlantılar tekrarlar veya koşullar arasında tekrarlanabilir mi? Tekrarlanabilirlik özgüven oluşturur.
✔ Bağlantılar belirli bölgelerde kümelenir mi? Kümeleme genellikle gerçek arayüzlere işaret eder.
✔ Mutant/ligand koşulları bağlantı desenini değiştirir mi? Değişimler mekanizmayı ortaya çıkarabilir.
Sonra kanıtları sonraki adımlara dönüştürün. Bağlantılar belirli bir arayüzü destekliyorsa, doğrulama için nokta mutasyonları tasarlayabilirsiniz. Eğer bağlantılar beklenmedik partnerler öneriyorsa, ortogonal onay planlayabilirsiniz. Bağlantılar bir modeli kısıtlıyorsa, yapısal iyileştirmeye daha yüksek güvenle geçebilirsiniz.
CTA: XL-MS ile Membran Proteinlerini Analiz Etmek İstiyorsanız ancak koşulları veya kontrolleri nasıl seçeceğinizden emin değilseniz, Longlight Technology ile iletişime geçip çapraz bağlama planı geliştirin ve sindirimden veri analizine kadar tam bir iş akışı raporu alın. Projenize net, yeni başlayanlar için uygun bir deneysel yol haritasıyla başlamak için ücretsiz bir teklif alın.
Neden Longlight Teknolojisi fveya XL-MS and Beyond
Zar protein projeleri nadiren tek bir teknikte yaşar. Genellikle platform zihniyeti gerektirirler: güvenilir örnek işleme, titiz veriler ve yinelemeyi hızlandıran araçlar.
Longlight Teknolojisi, modern laboratuvarlarda verimlilik ve doğruluğu artırmak için tasarlanmış ileri genomik çözümleri, gelişmiş laboratuvar aletleri ve yüksek kaliteli reaktifler ve tüketim malzemeleriyle her yönden destek sağlar. XL-MS hizmetlerinin yanı sıra, araştırma ekiplerine genomik ve moleküler biyoloji araçları dahil; bunlar arasında odaklı ultrasonikasyon sistemleri gibi NGS ile ilgili aletler ve akademik, klinik ve endüstriyel uygulamalar için yaygın kullanılan tüketim malzemeleri ve kitler (precast agaroz jelleri, nüklein asit ekstraksiyon kitleri ve kütüphane hazırlık kitleri) bulunmaktadır.
XL-MS ile Membran Proteinlerini Analiz Etmek sadece bir yöntem değil—bu bir iş akışı disiplinidir. İş akışı stabil olduğunda, sonuçlarınız daha netleşiyor, modelleriniz daha savunulabilir hale geliyor ve bir sonraki deneyiniz tasarlanması daha kolay hale geliyor.