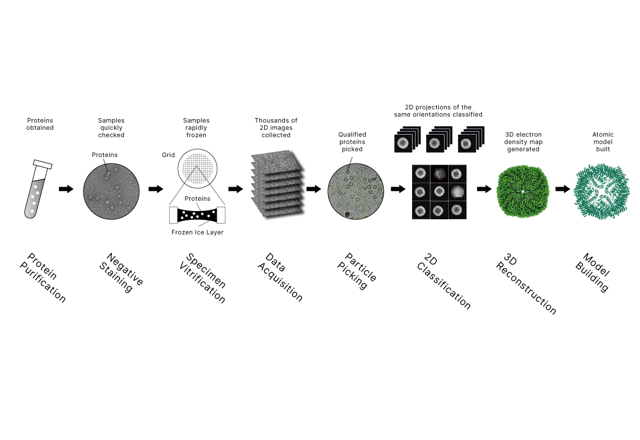
İlgili Yazı
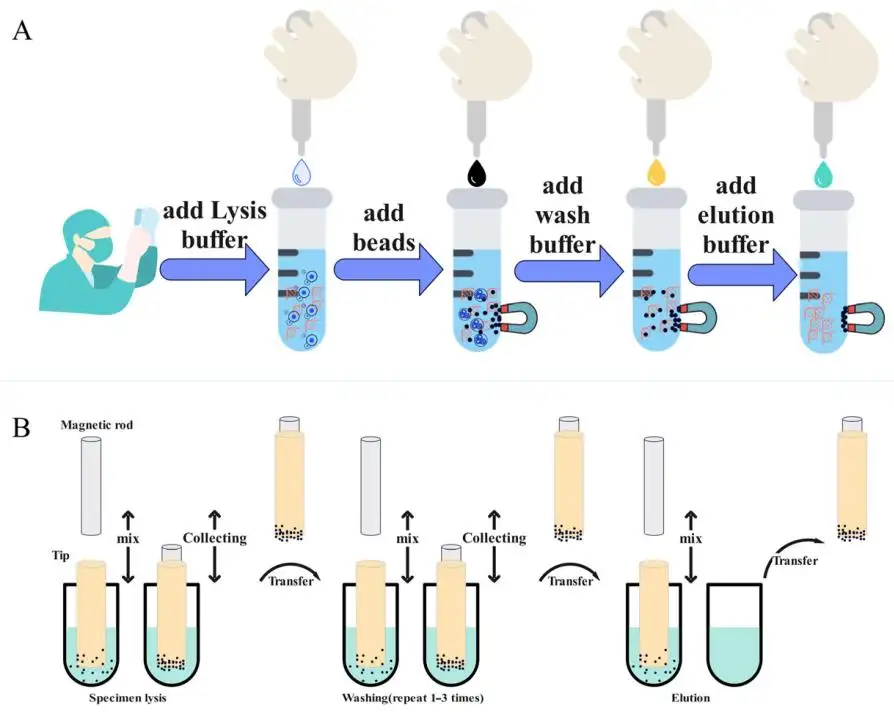
Nuklein Asit Arıtması için Manyetik Separatör: Daha Akıllı Ölçeklendirme Temizleme İş Akışlarının Daha İyi Çalışmasına Nasıl Yardımcı Olur
2026-03-26

Elektroforez görüntüleme sisteminizi ne bozuyor?
2025-08-19
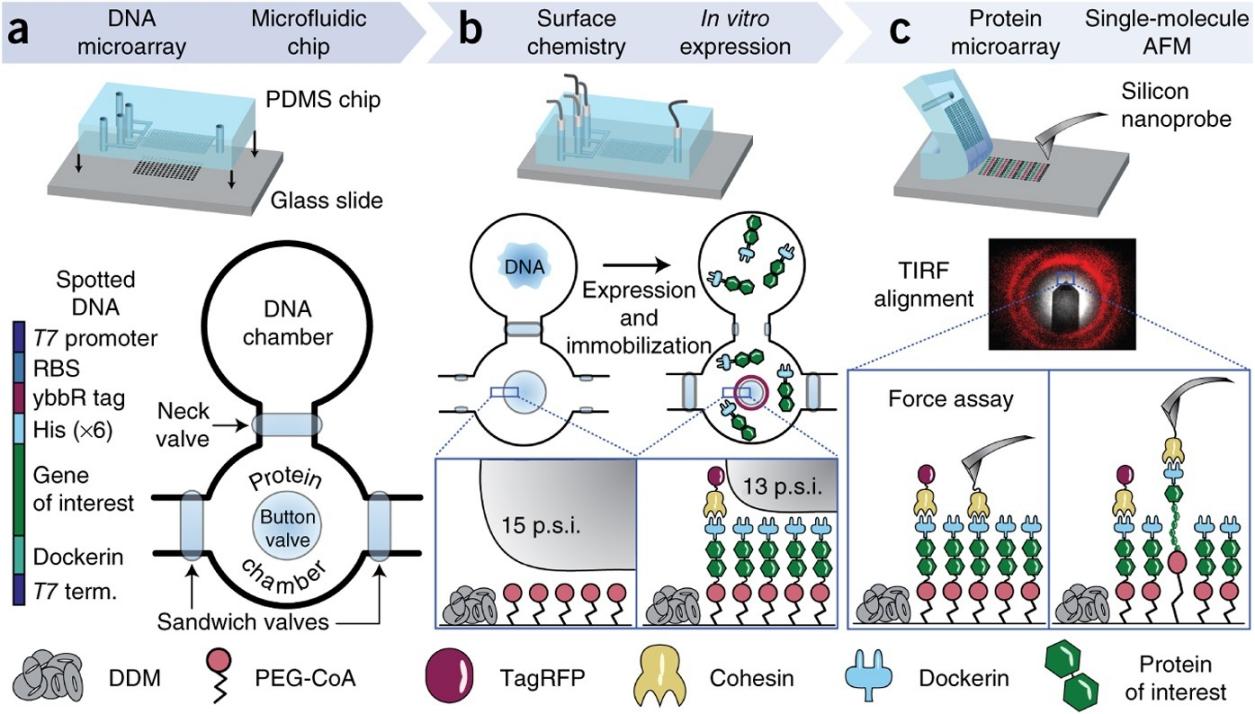
ChIP: Proteinlerin Genleri Nasıl Kontrol Ettiğini Ortaya Koymak: Basit Bir Soruyla Başlıyor
2026-02-25
Protein kompleksleri için çapraz bağlama MS'nin konformasyonel değişim hakkında ne öğrettiğini
2026-02-22Protein Kompleksleri için Çapraz Bağlama MS, gerçek protein temaslarını yerinde "dondurmanın" ve ardından bunları kütle spektrometrisiyle okumanın en pratik yollarından biridir—böylece bir kompleksin şeklini nasıl değiştirdiğini öğrenebilirsiniz, sadece tek bir anlık görüntüde nasıl göründüğünü değil. Longlight Technology'de birçok ekip basit bir soruyla başlıyor: Protein kompleksim statik mi, yoksa işlev için önemli olan konformasyonlar arasında geçiş mi yapıyor? Bu makale, kimyasal çapraz bağlamanın kütle spektrometrisi (genellikle CL-MS veya XL-MS olarak adlandırılır) ile birleştiğinde konformasyonel değişim hakkında size ne öğretebileceğini ve sonuçları nasıl harekete geçirebileceğiniz kararlara dönüştürülebileceğini yeni başlayanlar için uygun bir şekilde açıklıyor.
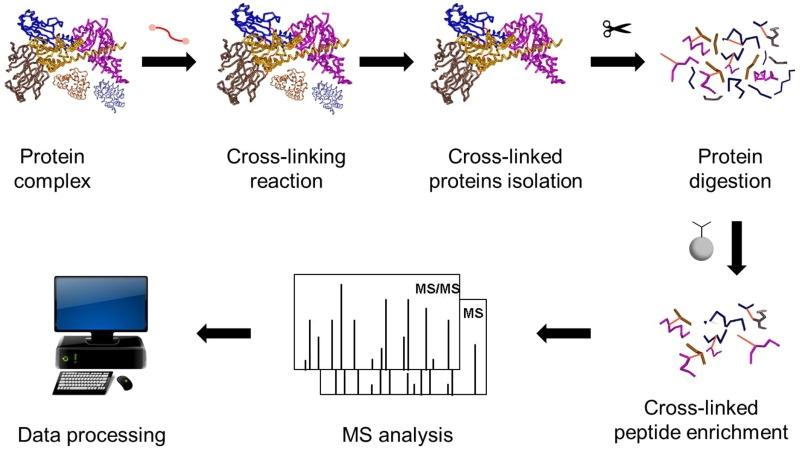
Kimyasal çapraz bağlama ve kütle spektrometrisi ile protein kompleks analizindeki gelişmeler
1) Çapraz Bağlama MS nedir?
Çapraz Bağlama MS (genellikle XL-MS veya CL-MS olarak yazılır) Proteinlerin hangi parçalarının birbirine yakın olduğunu bulmanıza yardımcı olan bir yöntemdir—ister bir protein içinde ister bir kompleksteki proteinler arasında—kimyasal olarak "bağlanarak" ve ardından bu bağlantıları kütle spektrometrisiyle tespit eder.
İşte fikir sade İngilizce:
• Çapraz bağlayıcı (küçük bir kimyasal "köprü") ekleyin
Belirli amino asitlerle reaksiyona girer ve birbirine sınırlı mesafede olan iki kalıntıyı kovalent olarak bağlayabilir.
• Proteinleri peptitlere dönüştürür
Enzimler (genellikle tripsin) proteinleri daha küçük parçalara böler.
• Kütle spektrometrisi
MS, çapraz bağlı peptit çiftleri dahil olmak üzere peptidleri tespit eder.
• Çapraz bağlantıları analiz edin
Her tanımlanan çapraz bağlantı bir mesafe kısıtlaması haline gelir:
"Kalıntı A ve kalıntı B bu koşullarda birbirine bağlanacak kadar yakındı."
Ne amaçla kullanıldığı
• Protein–protein etkileşimi (PPI) haritalama: bir komplekste kimin kime dokunduğu
• Arayüz tanımlama: temas yüzeyini oluşturan bölgeler
• Konformasyon değişimi: koşulları karşılaştırın (apo vs ligand-bağlı, mutant vs WT) ve kontaktların ortaya çıkıp kaybolduğunu görmek
• Yapısal modellemeyi desteklemek: modelleri doğrulamak veya geliştirmek için kriyo-EM/X-ışını ile birleştirerek
Neden değerli olduğu
• Zayıf veya kısa ömürlü etkileşimleri yakalayabilir (kovalent bağlantı onları "dondurur")
• Çoğu zaman özel etiketleme gerekmez
• Birden fazla koşulu karşılaştırmak için nispeten yüksek verimliliğe sahip olabilir
2) Konformasyonel Değişim Neden Bu Kadar Zor To Yakalama
Birçok protein kompleksi hareketsiz durmaz. Ligandlara, tuza, pH, fosforilasyona veya bağlanma partnerlerine yanıt olarak nefes alır, döner, açılır, kapanır ve alt birimleri yeniden düzenler. Geleneksel yapısal yöntemler mükemmel olabilir, ancak genellikle kararlı durumları tercih ederler. Bir kompleks esnekse, zayıf monte edilmiş veya kısa ömürlüyse, hikayenin sadece bir kısmını görebilirsiniz.
Çapraz bağlama yardımcı olur çünkü belirli bir mesafede olan iki kalıntıyı kovalent olarak bağlayabilir. Açık dilde, tepki anında "bu iki pozisyon birbirine dokunacak kadar yakındı" anlamına gelir. Yan yana çapraz bağlantı karşılaştırmaları—ligandsız mı yoksa bağlanmış, düşük ve yüksek tuzlu, vahşi tip ve mutant—kompleksin sıkıştırıp genişlemeyeceğini, yoksa yeniden yapılandırılıp yapılmadığını gösterir.
✅ Yeni başlayanlar için pratik bir bilgi: konformasyonel değişimler topluluk değişimleridir. XL-MS, en kararlı konformasyonun ötesine çözümdeki durumların spektrumuna kadar görür.
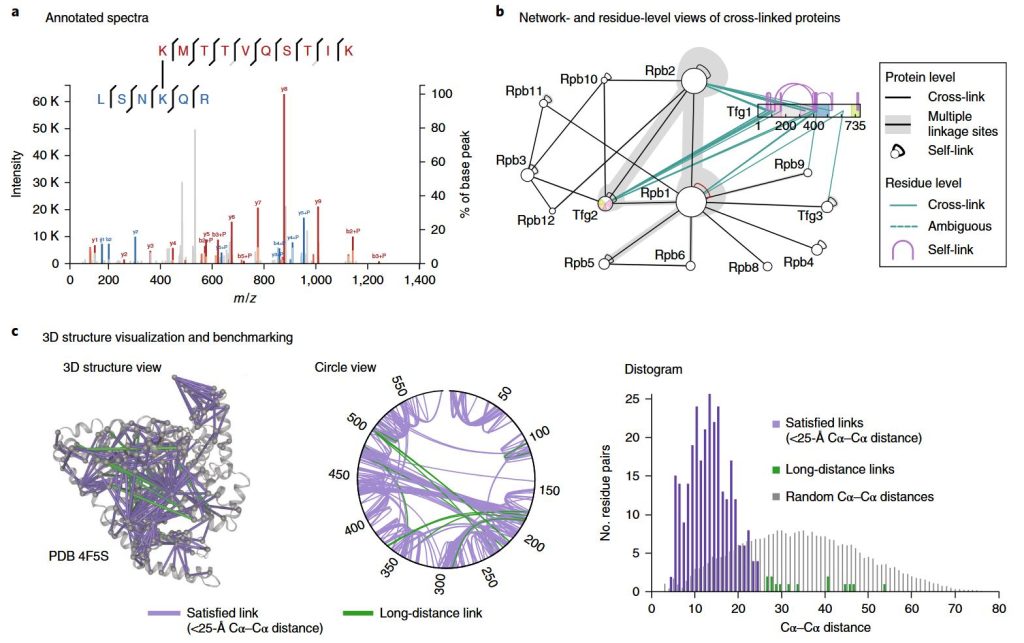
Çapraz Bağlama Kütle Spektrometrisi Hizmeti | MtoZ Biolabs
Çapraz Bağlama MS'nin Pratikte Hangi Ölçümleri Ölçer?
MS ile kimyasal çapraz bağlama, kalıntı yakınlığını ve etkileşim desenlerini nicelikten ölçer; bu, PPI'ların incelenmesi için standart bir yaklaşımdır. Çapraz bağlama ajanları, proteinler üzerindeki fonksiyonel gruplarla reaksiyona girer ve iki veya daha fazla etkileşimli proteini (veya bir protein içinde iki pozisyonu) bağlayabilir. Çapraz bağlamadan sonra, kütle spektrometrisi çapraz bağlı peptitleri analiz eder; böylece etkileşim ağlarını tasvir edebilir ve eylem noktalarını tespit edebilirsiniz.
Bu, konformasyonel değişim için ne anlama geliyor?
• Bir çapraz bağlantı kümesi yalnızca ligand bağlanmasından sonra ortaya çıkarsa, bağlı durumda yeni temasların oluştuğunu gösterir.
• Bazı çapraz bağlantılar kaybolursa, bu sitelerin artık yakın olmadığını gösterir—belki kompleks açılır ya da bir alan taşınır.
• Alt birimler arasında çapraz bağlantılar kayıyorsa, bu alt birimin yeniden düzenlenmesini veya farklı bir montaj yolunun olduğunu gösterebilir.
✅ Bu yöntemden ne kazanırsınız (ve neden önemli):
• Özel kimyasal etiketleme gerekmez → proteininizi doğal formuna yakın tutabilir ve deneysel yükü azaltabilirsiniz.
• Kısa ömürlü/zayıf etkileşimleri yakalar → kovalent bağlar, arındırma veya analiz sırasında dağılan temasları koruyabilir.
• Yüksek verimlilik ve hızlı analiz hızı birçok koşul veya yapıyı verimli şekilde karşılaştırmanız → faydalıdır.
• Hücre içi çapraz bağlama mümkündür → bazı projeler için bu, kompleksleri sadece in vitro değil, kendi doğal hücresel bağlamlarına daha yakın incelemenize yardımcı olur.
4) Okuma "Hareket" Çapraz Bağlantı Desenlerinden
Yeni başlayanlar bazen bir çapraz bağlantının bir cevap eşit olduğunu düşünür. Pratikte, değer kalıplardan gelir.
Düşünmek için faydalı bir yol şudur: çapraz bağlantılar mesafe kısıtlamalarıdır. Bir kompleks konformasyon değiştirdiğinde, iki kalıntı arasındaki mesafe de değişir. XL-MS her zaman tam dönüş açısını söyleyemez, ancak bölgelerin muhtemelen daha yakın mı yoksa daha da uzaklaştığını ve etkileşim haritasının değişip değişmediğini söyleyebilir.
XL-MS'nin ortaya çıkarabileceği yaygın konformasyon hikayeleri şunlardır:
✅ Sıkıştırma vs Açılış
Bir koşul altında uzak bölgeleri kapsayan daha fazla protein içi çapraz bağlantı görürseniz, protein daha kompakt bir durum benimsemiş olabilir. Eğer bu bağlantılar düşerken diğerleri yükselirse, açılıyor olabilir.
✅ Arayüz Anahtarlama
Alt birimi A ile B arasındaki çapraz bağlantılar zayıflarken A ve C arasındaki bağlantılar güçlenirse, bu yeniden ağırlıklandırılmış bir montaj veya arayüz anahtarı önerir.
✅ Ligand veya Mutasyonla Stabilizasyon
Bir konformasyonu "kilitleyen" bir ligand, belirli bir çapraz bağlantı kümesinin tekrarlanabilirliğini artırır ve karışık desenleri azaltır.
Pratikte bakıldığında, bu sonraki adımları yönlendirebilir: hangi mutantın yapılacağı, hangi alanın kesileceği, hangi tampon koşulu kompleksi stabilize edecek veya hangi arayüzün başka bir yöntemle doğrulanacağı yönünde.
5) XL-MS kriyo-EM veya X-ışın ile birleştirildiğinde daha güçlü sonuçlar
XL-MS, biyolojik yapı araştırmalarında sıklıkla kriyoelektron mikroskopisi (kriyo-EM) ve X-ışını kristal kırınımı ile birlikte kullanılır. Bu kombinasyon özellikle konformasyon değişikliği temel soru olduğunda faydalıdır.
• Kriyo-EM, baskın durumlar için yapısal bir model sağlayabilir.
• XL-MS, bir modelin çözüm davranışıyla tutarlı olup olmadığını doğrulayabilir ve kriyo-EM'nin eksik örneklediği alternatif durumları işaretleyebilir.
• X-ray yüksek çözünürlüklü alanlar sağlayabilirken, XL-MS alanları esnek bir montaj içinde yerleştirmeye yardımcı olur.
✅ Pratik bir iş akışı: önce XL-MS kullanarak kompleksinizin heterojen olup olmadığını öğrenin. Eğer öyleyse, yüksek çözünürlüklü yapı çalışmalarına büyük yatırım yapmadan önce bir eyaleti zenginleştiren koşullar tasarlayabilirsiniz.
6) Hizmet İş Akışı At Longlight Teknolojisi
Birçok laboratuvar, Protein Kompleksleri için Çapraz Bağlama MS'in içgörülerini tam bir üretim hattı inşa etmeden almak ister. Longlight Technology, hem deneyimli ekipleri hem de ilk kez kullanıcıları net bir hizmet süreciyle destekliyor.
Çapraz bağlantılı örnekler gönderebilir veya bizimle iletişime geçip çapraz bağlama planı geliştirip numune gönderebilirsiniz. Enzim sindirimi, peptid zenginleştirme, kütle spektrometrisi tespiti, veri analizi ve deneysel raporun teslim edilmesi dahil olmak üzere tam iş akışını tamamlarız. Bu uçtan uca yaklaşım önemlidir çünkü konformasyonel yorum, adımlar arasında tutarlı bir şekilde ele geçirilmeye bağlıdır.
✅ Bu sizin için müşteri olarak ne anlama geliyor:
• Adımlar arasında daha az handoff hatası ve koşulları karşılaştırdığınızda daha az "bilinmeyen"
• Sadece ham tanımlamalar değil, eyleme uygun yorum etrafında organize edilmiş bir rapor
• Birden fazla yapıyı veya tedavi koşullarını test etmeniz gerektiğinde daha hızlı yineleme
Daha geniş projeniz genomik veya üst yönlü analiz geliştirmeyi içeriyorsa, Longlight ayrıca modern laboratuvarlarda verimlilik ve doğruluğu artırmak için tasarlanmış ileri düzey genomik çözümleri, gelişmiş laboratuvar aletleri ve yüksek kaliteli reaktifler ve tüketim malzemeleri sunar—moleküler biyolojiden hassas analize kadar araştırma iş akışlarını destekler.
7) Pratik bir CTA: Konformasyon Sorularını Testlenebilir Kanıta Dönüştürün
Konformasyon değişikliği yan detay değildir. Genellikle bir hedefin ilaçlanabilir olup olmadığına, bir kompleksin doğru şekilde yapıp oluşmadığına ve mutasyonun gerçekten bozucu olup olmadığına karar verir. Protein Kompleksleri için Çapraz Bağlama MS'i, koşullar arasında karşılaştırabileceğiniz kanıtlar sunar, bu da tahmin etmeyi bırakıp tasarım yapmaya başlamanıza yardımcı olur.
✅ Eğer bir konformasyonel değişim çalışması planlıyorsanız, bir "karşılaştırma seti" ile başlamayı düşünün:
• Apo vs ligand-bağlı (veya inhibitör-bağlı)
• Vahşi tip ve tek arayüzlü mutant
• Bir stabilizator tampon vs bir stres tamponu (tuz/pH aralığı)
CTA: Protein kompleksinize göre net, yeni başlayanlar için uygun bir XL-MS planı istiyorsanız, hedefinizi (etkileşim haritalama, arayüz doğrulama veya konformasyon karşılaştırması) görüşmek için Longlight Technology ile iletişime geçin. Pratik çapraz bağlama stratejisi seçmenize ve bir sonraki deneyinizi veya bir sonraki yapısal modelinizi destekleyecek yorumlanabilir bir rapor sunmanıza yardımcı olabiliriz.